Trudno znaleźć inny proces biologiczny, który z taką konsekwencją podkopuje podstawy zdrowia jak przewlekły stres oksydacyjny. To on, cicho i systematycznie, rozregulowuje równowagę redox, prowadząc do uszkodzeń mitochondriów, białek, DNA i całych tkanek. Efekt? Zaburzona homeostaza komórkowa, wyczerpane rezerwy antyoksydantów endogennych i postępujące procesy starzenia, które rozpoznajemy często dopiero w wynikach badań lub pod postacią chorób przewlekłych.
W skrócie: konsekwencje stresu oksydacyjnego to nie tylko zmęczenie komórkowe, lecz także bezpośredni udział w rozwoju chorób neurodegeneracyjnych, miażdżycy i nowotworów. Coraz więcej badań zwraca uwagę na rolę wodoru cząsteczkowego w przywracaniu równowagi redox i modulacji stresu komórkowego. Jeśli chcesz poznać pełne zaplecze badań i mechanizmów działania, zajrzyj do strony mechanizmów działania terapii wodorem molekularnym.
- Wyjaśnienie, czym jest stres oksydacyjny i jak się rozwija
- Szczegółowe omówienie skutków uszkodzeń oksydacyjnych
- Analiza roli wodoru w regulacji mitochondriów i szlaków redox
- Omówienie badań z MDPI i PubMed
- Praktyczne wnioski dotyczące prewencji i bezpieczeństwa
Mechanizmy powstawania przewlekłego stresu oksydacyjnego i jego markery
W warunkach fizjologicznych równowaga między reaktywnymi formami tlenu a antyoksydantami endogennymi (takimi jak glutation, katalaza czy dysmutaza ponadtlenkowa) utrzymuje się na poziomie zapewniającym prawidłową funkcję komórek. Jednak ekspozycja na czynniki prooksydacyjne – stres środowiskowy, zanieczyszczenie powietrza, stres metaboliczny – może prowadzić do nadprodukcji rodników hydroksylowych i nadtlenku wodoru. Z czasem nadmiar tych form powoduje peroksydację lipidów i degradację struktur błonowych.
Badania in vitro wskazują, że długotrwała dysfunkcja mitochondrialna to kluczowe źródło reaktywnych form tlenu w komórkach. Utrata kontroli nad procesami redox prowadzi do uszkodzeń DNA, aktywacji szlaków zapalnych NF-κB i nadmiernej apoptozy komórek. Klinicznie obserwuje się wzrost markerów stresu oksydacyjnego takich jak 8-OHdG czy MDA. To zjawisko potwierdzają m.in. badania [MDPI](https://www.mdpi.com/1422-0067/25/14/7884) opisujące związek między oksydacją lipidów a degeneracją tkanek.
Identyfikacja biomarkerów stresu oksydacyjnego umożliwia ocenę skuteczności interwencji farmakologicznych i naturalnych antyoksydantów. W tym kontekście istotne są dane z badań klinicznych nad biomarkerami stresu oksydacyjnego, które określają poziomy markerów redox w odniesieniu do stanu klinicznego pacjenta.
| Marker | Rodzaj uszkodzenia | Znaczenie kliniczne |
|---|---|---|
| 8-OHdG | Uszkodzenia DNA | Ocena ryzyka nowotworowego |
| MDA | Peroksydacja lipidów | Stan zapalny naczyń |
| GSH/GSSG | Równowaga redox | Pomiar efektywności obrony antyoksydacyjnej |
| CAT | Aktywność antyoksydacyjna | Ocena pracy mitochondriów |
| NO• | Reaktywne formy azotu | Ocena stresu nitrozacyjnego |
Uszkodzenia oksydacyjne w tkankach — skutki długofalowe
Degeneracja neuronalna i choroby neurodegeneracyjne
Stres oksydacyjny w układzie nerwowym nasilony jest przez wysokie zużycie tlenu i obecność nienasyconych kwasów tłuszczowych w neuronach. Z czasem dochodzi do uszkodzeń białek synaptycznych, co obserwowano m.in. w chorobie Parkinsona i Alzheimera. Badania [PubMed](https://pubmed.ncbi.nlm.nih.gov/39653185/) wskazują, że molekularny wodór może utrzymywać homeostazę mitochondrialną i chronić neurony przed skutkami stresu oksydacyjnego.
Uszkodzenia śródbłonka i miażdżyca
W ścianach naczyń gromadzą się zmodyfikowane lipidy, które inicjują kaskadę zapalną i powstawanie blaszki miażdżycowej. Dodatkowo aktywacja reaktywnych form azotu nasila degenerację naczyń, co stwierdzono w badaniach nad przewlekłym stresem oksydacyjnym u pacjentów z nadciśnieniem i cukrzycą.
Dysfunkcja wątroby i stres metaboliczny
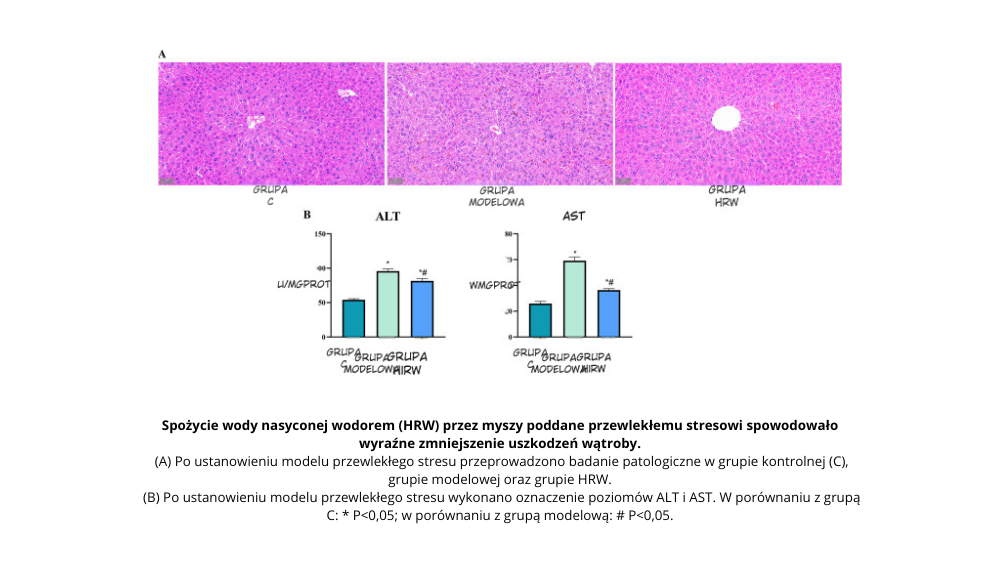
Eksperyment z wykorzystaniem wody bogatej w wodór u myszy poddanych chronicznemu stresowi wykazał poprawę kontroli mitochondrialnej i spadek markerów oksydacyjnych (PubMed, 2024, ID: 39951412). Wskazuje to na możliwą rolę wodoru w stabilizacji metabolicznej równowagi redox w wątrobie.
Peroksydacja lipidów i apoptoza komórek
Proces peroksydacji lipidów skutkuje nieodwracalnymi zmianami błon komórkowych, które mogą inicjować efekt cytotoksyczny i apoptozę. To zjawisko obserwowano w modelach nowotworowych, gdzie stres oksydacyjny działał jak swoiste narzędzie selekcji komórek.
Analizując te dane, można stwierdzić, że strategia prewencji obejmuje stosowanie antyoksydantów egzogennych i wspomagających terapii, takich jak wodór. Więcej w kontekście wspólnych działań opisano na stronie terapii antyoksydacyjnych z wykorzystaniem wodoru molekularnego.
Rola wodoru cząsteczkowego w utrzymaniu równowagi redox
Wodór cząsteczkowy jest unikalnym antyoksydantem, który reaguje selektywnie – neutralizuje najbardziej reaktywne formy tlenu, w tym rodniki hydroksylowe. Mechanistycznie jego działanie polega na hamowaniu łańcucha reakcji wolnorodnikowych, bez ingerencji w fizjologiczną sygnalizację komórkową. W modelach in vivo wykazano, że inhalacja wodoru poprawia parametry tlenowe i zmniejsza stres oksydacyjny w mózgu i wątrobie.
Ta wyjątkowa selektywna neutralizacja rodników czyni z niego czynną biologicznie cząsteczkę o wysokim potencjale terapeutycznym. W badaniach [MDPI](https://www.mdpi.com/2076-3921/13/7/856) połączenie wodoru i hemooksygenazy 1 skutecznie redukowało neuropatię indukowaną paklitakselem. Widać więc, że terapia wodorem może działać synergicznie z innymi mechanizmami detoksykacyjnymi organizmu.
W tabeli poniżej zestawiono najważniejsze mechanizmy działania wodoru molekularnego w kontekście stresu oksydacyjnego. Ciekawym rozszerzeniem tego zagadnienia są materiały dostępne pod adresem wolne rodniki i ich wpływ na metabolizm.
| Mechanizm | Efekt biologiczny | Poziom dowodu |
|---|---|---|
| Neutralizacja rodników •OH | Ochrona DNA i błon | RCT, 2023 |
| Regulacja NF-κB | Zmniejszenie stanu zapalnego | In vivo |
| Poprawa biogenezy mitochondriów | Odzyskanie homeostazy energetycznej | In vivo / mechanistyczne |
| Redukcja peroksydacji lipidów | Prewencja uszkodzenia błon komórkowych | Kliniczne |
| Stymulacja enzymów antyoksydacyjnych | Utrzymanie równowagi redox | RCT |
Potencjał terapii wodorem w kontekście chorób przewlekłych
Wodór w chorobach neurodegeneracyjnych
Badania wykazały, że inhalacja wodoru lub spożycie wody wodorowej może sprzyjać utrzymaniu homeostazy mitochondrialnej. W modelu CUMS (PubMed ID: 39653185) zaobserwowano poprawę funkcji poznawczych i spadek oksydacyjnych markerów zapalnych. To znaczący wniosek, który potwierdza, że wodór wspiera procesy naprawcze w neuronach.
Aplikacja wodoru w dermatologii oksydacyjnej
Badania [MDPI](https://www.mdpi.com/2076-3921/14/6/729) wykazały, że miejscowe stosowanie wody bogatej w wodór poprawia parametry skóry narażonej na stres oksydacyjny. Działa to poprzez zwiększenie aktywności antyoksydantów i poprawę jakości bariery lipidowej. Interesująco — efekt utrzymywał się nawet po kilku tygodniach od zakończenia terapii.
Molekularne działanie w układzie sercowo-naczyniowym
W modelach niedokrwienia/reperfuzji wodór zmniejszał obszar martwicy i hamował aktywację reaktywnych form azotu. W efekcie obserwowano poprawę perfuzji i redukcję stanu zapalnego (MDPI, 2024). Takie dane stanowią przesłankę do rozwoju wspomagających metod terapeutycznych dla pacjentów kardiologicznych.
W kontekście starzenia komórkowego odkrycia te nabierają jeszcze większego znaczenia — o czym więcej można przeczytać na stronie wolne rodniki a proces starzenia się.
Bezpieczeństwo i praktyczne aspekty stosowania wodoru
Choć wodór wykazuje korzystne właściwości przeciwzapalne i antyoksydacyjne, nie istnieją jeszcze pełne dane na temat jego długoterminowego stosowania. W badaniach krótkoterminowych nie odnotowano istotnych skutków ubocznych ani interakcji z lekami. Kluczowe jest jednak utrzymanie standardów czystości gazu i dokładne monitorowanie dawek – szczególnie przy podawaniu wodoru inhalacyjnie.
W terapii wspomagającej dla sportowców i pacjentów metabolicznych stosuje się obecnie wodór w napojach leczniczych i inhalacjach 2-4% stężeniem. Dawkowanie zależy od celu i stanu pacjenta – dlatego zawsze wymagana jest konsultacja specjalistyczna. Wodór powinien być pojmowany jako wsparcie terapii, a nie jej podstawowy element.
Jeśli interesuje Cię zaplecze technologiczne, warto zajrzeć na stronę urządzeń i technologii terapeutycznych opartych na wodorze.
Dlaczego warto dziś interesować się terapią wodorem?
Rozumienie stresu oksydacyjnego to nie tylko ciekawostka naukowa, ale podstawa zrozumienia procesów starzenia i chorób cywilizacyjnych. Wodór molekularny stanowi unikalny most pomiędzy światem biochemicznego chaosu a systemową równowagą redox. Działa subtelnie, lecz konsekwentnie — wspierając organizm w utrzymaniu homeostazy.
Dla firm i jednostek badawczych terapia wodorem to narzędzie przyszłości – ciche, ale wydajne. Jeśli chcesz poznać szczegóły współpracy czy włączyć technologię do praktyki medycznej, odwiedź stronę Polskiego Instytutu Terapii Wodorem Molekularnym.
Źródła
- The Protective Role of Molecular Hydrogen in Ischemia/Reperfusion Injury
- The Combination of Molecular Hydrogen and Heme Oxygenase 1 Effectively Inhibits Neuropathy Caused by Paclitaxel in Mice
- Topically Applied Molecular Hydrogen Normalizes Skin Parameters Associated with Oxidative Stress: A Pilot Study
- Long-term consumption of hydrogen-rich water provides hepatoprotection…
- Hydrogen restores central tryptophan and metabolite levels…
- Hydrogen-rich saline protects against oxidative damage and cognitive deficits…
FAQ
Czy wodór molekularny można przedawkować?
Nie ma dowodów na toksyczność wodoru w stosowanych dawkach terapeutycznych. Jego nadmiar wydychany jest w postaci gazowej. Jednak zbyt wysokie stężenia inhalacyjne (>4%) zwiększają ryzyko zapłonu, dlatego ważne jest stosowanie certyfikowanych urządzeń medycznych.
Jak długo trzeba stosować wodór, aby zauważyć efekty?
W badaniach klinicznych poprawa markerów stresu oksydacyjnego obserwowana była po 2–4 tygodniach. Czas ten zależy od formy podawania (inhalacja, woda wodorowa) i intensywności stresu metabolicznego organizmu.
Czy wodór działa na poziomie DNA?
Wodór sam w sobie nie wpływa bezpośrednio na sekwencję DNA, ale pośrednio chroni genom przed uszkodzeniami oksydacyjnymi neutralizując rodniki hydroksylowe.
Jakie grupy zawodowe korzystają z terapii wodorem?
Najczęściej stosują ją sportowcy, osoby pracujące w stresie oksydacyjnym i pacjenci w rekonwalescencji pooperacyjnej. Wykorzystuje się ją też jako profilaktykę u osób starszych.
Czy wodór może zastąpić suplementy antyoksydacyjne?
Nie. Wodór wspiera działanie antyoksydantów, ale nie zastępuje witamin C i E czy koenzymu Q10. Może natomiast wydłużać ich aktywność redox w komórkach.
Czy woda wodorowa ma trwałość działania?
Wodór szybko ulatnia się z roztworu (w ciągu 1–2 godzin), dlatego woda powinna być spożywana bezpośrednio po nasyceniu i przechowywana w zamkniętym naczyniu.
Jakie są przeciwwskazania do terapii wodorem?
Nie zaleca się jej osobom z ciężką niewydolnością oddechową lub po niedawnych zabiegach w obrębie układu oddechowego. Każdorazowo należy skonsultować się ze specjalistą posiadającym doświadczenie w tej metodzie.

