Każdego dnia nasze komórki stają wobec wyzwania, które choć niewidoczne, nieustannie wpływa na ich kondycję. Tym wyzwaniem jest stres oksydacyjny – stan zaburzenia równowagi pomiędzy produkcją reaktywnych form tlenu (ROS) a zdolnością organizmu do ich neutralizacji. Jego źródła są zarówno wewnętrzne, jak i zewnętrzne, a skutki odczuwamy dosłownie w każdej tkance, w każdym procesie metabolicznym.
W skrócie: stres oksydacyjny i rodniki powstają naturalnie w organizmie jako uboczny efekt oddychania komórkowego. Problem zaczyna się w momencie, gdy czynniki środowiskowe — takie jak promieniowanie UV, dym tytoniowy, pestycydy czy dieta wysokotłuszczowa — powodują nadprodukcję tych reaktywnych cząsteczek. W dalszej części wyjaśniam, skąd biorą się rodniki, jak wpływają na procesy komórkowe i w jaki sposób interwencje, jak np. terapia wodorem molekularnym, mogą wspierać utrzymanie równowagi redox.
W tekście znajdziesz:
- Wyjaśnienie biologicznych i środowiskowych źródeł stresu oksydacyjnego,
- Przegląd mechanizmów uszkodzeń oksydacyjnych DNA, białek i lipidów,
- Dane z metaanaliz oraz badań klinicznych dotyczących biomarkerów stresu oksydacyjnego,
- Analizę roli enzymów antyoksydacyjnych i naturalnych antyoksydantów,
- Omówienie potencjału wodoru molekularnego jako czynnika wspomagającego równowagę redox.
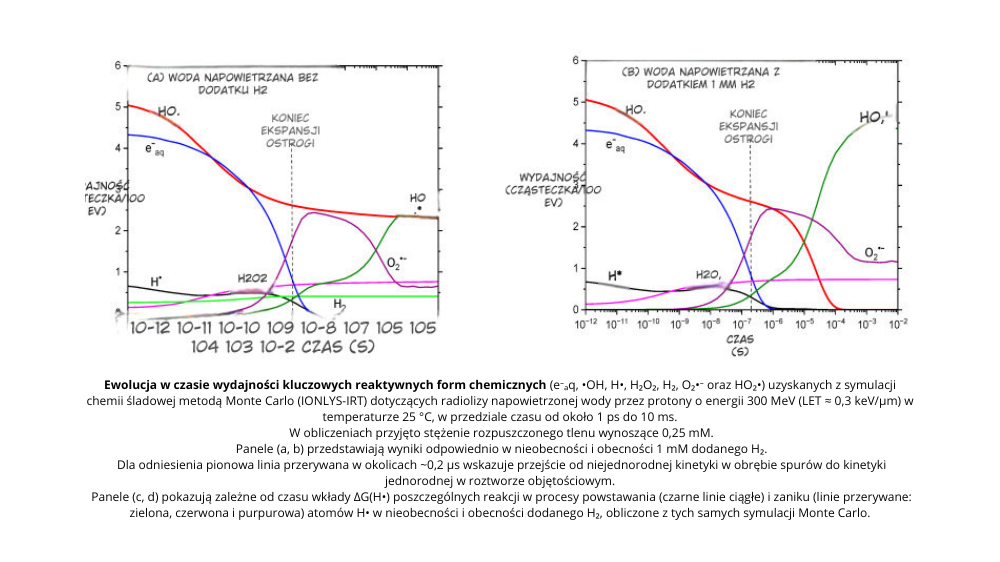
Endogenne źródła stresu oksydacyjnego: mitochondria, enzymy i procesy metaboliczne
Najważniejsze wewnętrzne źródło reaktywnych form tlenu stanowią mitochondria, a właściwie ich łańcuch oddechowy. W czasie przenoszenia elektronów przez kompleksy białkowe część z nich „ucieka” i reaguje z tlenem, tworząc nadtlenek wodoru (H₂O₂), rodniki hydroksylowe (•OH) oraz tlen singletowy (¹O₂). Choć w niewielkich ilościach ROS wspierają sygnalizację komórkową, ich nadmiar prowadzi do uszkodzenia DNA, peroksydacji lipidów i zaburzeń w funkcjonowaniu enzymów mitochondrialnych.
Drugim źródłem wewnątrzkomórkowym są enzymy takie jak oksydazy, cytochrom P450 i NADPH oksydaza — wszystkie związane z przemianami metabolicznymi i detoksykacją. W uszkodzonych lub przeciążonych komórkach, np. w hepatocytach czy neuronach, dochodzi do „rozregulowania” tych układów, co prowadzi do przewlekłego stresu oksydacyjnego. Badania z PubMed potwierdzają znaczenie tego zjawiska w patogenezie cukrzycy typu 2, miażdżycy, a także chorób neurodegeneracyjnych.
Istotnym czynnikiem jest również udział azotowych form reaktywnych (RNS) — w tym tlenku azotu (NO) i nadtlenoazotynu (ONOO⁻), które wchodząc w interakcje z ROS, nasilają uszkodzenia komórkowe. Nadmierne ilości RNS, w połączeniu z zaburzeniem działania enzymów takich jak dysmutaza ponadtlenkowa (SOD), katalaza (CAT) czy peroksydaza glutationowa (GPx), powodują trwałe zmiany w strukturze białek i fosfolipidów błon komórkowych.
| Źródło wewnętrzne | Rodzaj reaktywnej formy | Skutek | Poziom dowodów | Powiązane choroby |
|---|---|---|---|---|
| Łańcuch oddechowy mitochondriów | O₂•⁻, H₂O₂ | Uszkodzenie DNA mitochondrialnego | Meta-analiza | Choroba Parkinsona |
| Enzymy oksydacyjne | O₂•⁻ | Utlenianie lipidów błon | RCT | Miażdżyca |
| Cytochrom P450 | ¹O₂ | Nadmierna oksydacja substratów | Eksperymentalne | Uszkodzenie wątroby |
| NO syntaza | ONOO⁻ | Modyfikacja białek | In vivo | Cukrzyca typu 2 |
| Makrofagi aktywowane | H₂O₂ | Zaburzenie sygnalizacji NF-κB | Mechanistyczne | Stan zapalny |
Warto zrozumieć, że równowaga redox to nie statyczny stan — to dynamiczna równowaga pomiędzy wytwarzaniem a neutralizacją rodników. Kiedy ten balans ulega przesunięciu, powstaje efekt domina, prowadzący do szeregu reakcji oksydacyjnych w tkankach. Więcej o tym, jak chroniczny stres oksydacyjny oddziałuje na organizm, znajdziesz w sekcji: konsekwencje przewlekłego stresu oksydacyjnego.
Egzogenne źródła stresu oksydacyjnego: czynniki środowiskowe i styl życia
Choć organizm sam wytwarza ROS, większość przypadków przewlekłego stresu oksydacyjnego wynika z wpływu środowiska. Zanieczyszczenia powietrza, dym tytoniowy, metale ciężkie czy pestycydy generują nadmierne ilości rodników, które przenikają przez błony komórkowe i osłabiają mechanizmy obronne organizmu. Szczególnie toksyczny wpływ mają cząsteczki PM2.5, które w połączeniu z ozonem nasilają peroksydację lipidów w płucach.
Kolejne źródło to promieniowanie UV oraz promieniowanie jonizujące. Prowadzą one do powstawania rodników hydroksylowych, które atakują DNA i mogą powodować mutacje. Nie wolno zapominać o roli diety: przetworzona żywność, alkohol etylowy i dieta wysokotłuszczowa nasilają produkcję ROS w hepatocytach, podczas gdy niedobór snu i przewlekły stres psychiczny obniżają produkcję enzymów antyoksydacyjnych, takich jak SOD czy GPx.
Wpływ zanieczyszczeń i chemikaliów
Zanieczyszczenia wody, chemikalia przemysłowe czy pestycydy powodują długofalowe gromadzenie się toksyn w tkankach. Ich bioakumulacja prowadzi do mutacji mitochondrialnych i aktywacji szlaków sygnałowych prooksydacyjnych, m.in. NF-κB i MAPK. W badaniach z MDPI zauważono istotny związek między ekspozycją na ołów a wzrostem markerów stresu oksydacyjnego, takich jak MDA i 8-OHdG.
Stres psychiczny i fizyczny
Przewlekły stres i nadmierny wysiłek fizyczny zwiększają produkcję kortyzolu oraz adrenaliny, które pobudzają mitochondria do zwiększonego obrotu energetycznego. Proces ten, choć naturalny, przy braku adekwatnej regeneracji prowadzi do wzrostu ROS. Niedobór snu i brak równowagi między wysiłkiem a odpoczynkiem skutkują obniżeniem poziomu endogennych antyoksydantów, jak witamina C, witamina E czy koenzym Q10.
Wszystkie te czynniki działają synergistycznie, powodując, że organizm nie jest w stanie przywrócić równowagi redox. Jeśli interesuje Cię, jak to zjawisko mierzy się w praktyce klinicznej, zobacz sekcję: biomarkery stresu oksydacyjnego w badaniach klinicznych.
Mechanizmy obronne: enzymy antyoksydacyjne i rola antyoksydantów dietetycznych
Ciało człowieka ma rozbudowany system obronny przed nadmiarem rodników. W jego skład wchodzą enzymy antyoksydacyjne – m.in. dysmutaza ponadtlenkowa, katalaza i peroksydaza glutationowa – które przekształcają ROS w mniej reaktywne formy, głównie wodę i tlen. Wspomagają je antyoksydanty nieenzymatyczne: witamina C, witamina E, glutation oraz koenzym Q10. Ich synergia decyduje o integralności komórkowej i o tym, jak skutecznie organizm radzi sobie z oksydacyjnym uszkodzeniem.
W jednej z metaanaliz (MDPI, 2024) wykazano, że suplementacja przeciwutleniaczy może wspomagać funkcję śródbłonka, jednak skuteczność zależy od wyjściowego poziomu stresu oksydacyjnego. W stanach patologicznych, jak miażdżyca czy choroba Alzheimera, działanie antyoksydantów bywa osłabione przez zaburzoną ekspresję genów antyoksydacyjnych (np. Nrf2).
| Antyoksydant | Mechanizm działania | Poziom dowodów | Źródło naturalne | Efekt biologiczny |
|---|---|---|---|---|
| Witamina C | Redukcja H₂O₂ | RCT | Owoce cytrusowe | Wzmacnia regenerację glutationu |
| Witamina E | Przerywanie peroksydacji lipidów | Meta-analiza | Orzechy, oleje roślinne | Ochrona błon komórkowych |
| Koenzym Q10 | Transport elektronów w mitochondriach | RCT | Mięso, ryby | Wspiera produkcję energii ATP |
| Glutation | Redukcja nadtlenków lipidowych | In vivo | Warzywa krzyżowe | Detoksykacja komórkowa |
| Peroksydaza glutationowa | Usuwanie H₂O₂ | RCT | Endogenny enzym | Utrzymanie równowagi redox |
Część badań (np. MDPI, 2024) podkreśla, że enzymy SOD, CAT i GPx działają wspólnie, a niewydolność jednego z nich zwiększa wrażliwość komórek na ROS. Szczególnie interesujące są analizy nad aktywacją szlaku Nrf2, którego modulacja przez wodór molekularny może oferować nową strategię terapeutyczną — o czym więcej w artykule terapie antyoksydacyjne a wodór molekularny.
Wpływ stresu oksydacyjnego na choroby i starzenie się organizmu
Stres oksydacyjny przyspiesza proces starzenia się komórek i stanowi wspólny mianownik dla wielu chorób cywilizacyjnych. W tkankach nerwowych prowadzi do akumulacji uszkodzeń DNA, w mięśniach sercowych – do utraty potencjału mitochondrialnego, a w trzustce – do zaburzeń wydzielania insuliny. Badania naukowe (PubMed, 2023) wskazują, że przewlekłe uszkodzenia oksydacyjne są jednym z głównych czynników rozwoju choroby Alzheimera, Parkinsona oraz nowotworów złośliwych.
Nie bez znaczenia pozostaje wpływ ROS na układ sercowo-naczyniowy. Nadmiar tlenku azotu i nadtlenku wodoru sprzyja powstawaniu oksydowanego LDL, inicjując proces miażdżycy. W przypadku cukrzycy typu 2, stres oksydacyjny obniża wrażliwość komórek na insulinę, nasilając insulinooporność. Wykazano, że ograniczenie ekspozycji na czynniki środowiskowe i zwiększenie spożycia antyoksydantów może obniżać poziom markerów ROS o 25–40%, zależnie od wieku i płci badanych (MDPI, 2024).
Mechanizmy w chorobach neurodegeneracyjnych
W mózgu stres oksydacyjny oddziałuje z zapalnymi szlakami sygnałowymi, prowadząc do degeneracji neuronów dopaminergicznych (choroba Parkinsona) lub akumulacji amyloidu (choroba Alzheimera). Słaba regeneracja glutationu i niski poziom katalazy sprawiają, że neurony są szczególnie wrażliwe na ROS. Badania in vivo potwierdzają, że zastosowanie selektywnych antyoksydantów, jak wodór molekularny, może spowalniać ten proces.
Choroby serca i metaboliczne
W kardiomiocytach ROS przyczyniają się do dysfunkcji mitochondriów i zaburzeń rytmu serca. Z kolei w adipocytach nasilają stan zapalny niskiego stopnia, co prowadzi do rozwoju insulinooporności. Interwencje dietetyczne i farmakologiczne mają na celu ograniczenie ROS i przywrócenie równowagi redox, choć skuteczność tych strategii nadal jest przedmiotem intensywnych badań (PubMed, 2024).
Warto zrozumieć, że żaden pojedynczy mechanizm nie tłumaczy całości zjawiska stresu oksydacyjnego — to konglomerat czynników genetycznych, środowiskowych i metabolicznych. W rozdziale poświęconym wolnym rodnikom wyjaśniam dokładniej, jakie ich rodzaje dominują w konkretnych chorobach i jak można je modulować.
Znaczenie równowagi redox i perspektywy terapii wspierających
Utrzymanie równowagi redox to nie tylko kwestia zdrowia komórkowego — to podstawowy warunek homeostazy całego organizmu. Interwencje wspierające antyoksydacyjnie, w tym zastosowanie terapii wodorem molekularnym, są obiecującym kierunkiem badań. W publikacji MDPI (2024) opisano, że wodór selektywnie neutralizuje rodniki hydroksylowe, nie zakłócając fizjologicznych funkcji ROS w sygnalizacji komórkowej.
Badania in vitro oraz RCT potwierdzają, że wodór może działać jako dodatkowy element wspierający tradycyjne strategie antyoksydacyjne. Zaobserwowano redukcję markerów stresu oksydacyjnego (np. MDA, 8-OHdG) oraz modulację ekspresji genów antyoksydacyjnych przez aktywację szlaku Nrf2. Choć terapia ta nie zastępuje leczenia podstawowego, może pełnić rolę komplementarną w profilaktyce chorób oksydacyjnych.
Równowaga redox to również styl życia – sen, aktywność, dieta, unikanie toksyn. W skrócie: jeśli rozumiemy mechanizm stresu oksydacyjnego, możemy go świadomie ograniczać. Nie ma jednej recepty, ale istnieje wiele narzędzi — o części z nich przeczytasz w praktycznych zastosowaniach terapii wodorem molekularnym.
Jak wykorzystać tę wiedzę w praktyce
Tak naprawdę każdy z nas jest codziennie wystawiony na działanie czynników oksydacyjnych. Ale mając świadomość, czym są rodniki, jak działają mitochondria i w jaki sposób dieta czy sen wpływają na równowagę redox — możemy działać prewencyjnie. Wodoroterapia, dieta bogata w antyoksydanty, umiarkowany ruch i redukcja ekspozycji na toksyny tworzą wspólne podłoże dla ochrony komórek.
Wiedza ta staje się fundamentem nie tylko profilaktyki, ale i świadomego stylu życia. Zachęcam, by odwiedzić naszą stronę Polskiego Instytutu Terapii Wodorem Molekularnym, gdzie znajdziesz zarówno najnowsze publikacje, jak i praktyczne rekomendacje dotyczące wspierania równowagi redox w codzienności.
Źródła
- The Protective Role of Molecular Hydrogen in Ischemia/Reperfusion Injury
- Oxidative Stress: The Role of Antioxidant Phytochemicals in the Prevention and Treatment of Diseases
- Cellular ROS and Antioxidants: Physiological and Pathological Role
- Free Radicals and Oxidative Stress: Signaling Mechanisms, Redox Basis for Human Diseases, and Cell Cycle Regulation
- Molecular Hydrogen as an Antioxidant and Radioprotector
- Molecular Hydrogen Protects Human Melanocytes from Oxidative Stress by Activating Nrf2 Signaling
FAQ
Jak można zmierzyć stres oksydacyjny w organizmie?
Najczęściej wykorzystuje się biomarkery takie jak MDA, 8-OHdG, oksydowane LDL oraz wskaźniki aktywności enzymów antyoksydacyjnych (SOD, CAT, GPx). Pomiar może być wykonywany w krwi, moczu lub ślinie i pozwala na ocenę aktualnego poziomu stresu oksydacyjnego.
Czy suplementacja witaminami C i E zawsze jest korzystna?
Nie zawsze. Nadmiar przeciwutleniaczy może paradoksalnie zaburzać fizjologiczną sygnalizację ROS, zwłaszcza u osób zdrowych. Zawsze zaleca się indywidualną ocenę potrzeb organizmu.
Jaką rolę odgrywają mitochondria w procesie starzenia?
Mitochondria są źródłem energii, ale także głównym producentem ROS. Ich dysfunkcja prowadzi do akumulacji uszkodzeń DNA mitochondrialnego, co przyspiesza proces starzenia się komórek.
Czy wodór molekularny może zastąpić tradycyjne leczenie chorób oksydacyjnych?
Nie. Może natomiast pełnić funkcję wspierającą poprzez selektywną neutralizację rodników hydroksylowych i modulację szlaku Nrf2. Dalsze badania kliniczne są konieczne do oceny jego skuteczności w długim terminie.
Jakie choroby najczęściej wiąże się z przewlekłym stresem oksydacyjnym?
Do najczęstszych należą: miażdżyca, cukrzyca typu 2, choroba Alzheimera, Parkinsona, a także liczne nowotwory złośliwe. Wszystkie łączy nadmiar ROS i zaburzenia równowagi redox.
Czy aktywność fizyczna zwiększa stres oksydacyjny?
Tak, ale w sposób kontrolowany. Umiarkowany wysiłek fizyczny stymuluje naturalne mechanizmy obronne i podnosi poziom endogennych enzymów antyoksydacyjnych, podczas gdy przetrenowanie może działać odwrotnie.
Jakie produkty spożywcze wspierają równowagę redox?
Największe korzyści przynoszą świeże warzywa, owoce, orzechy, ziarna, oliwa z oliwek, a także produkty bogate w polifenole. Dieta śródziemnomorska jest uznawana za model wspierający równowagę redox i ochronę mitochondriów.

