Każdy organizm, od pojedynczej komórki po złożony układ człowieka, żyje w równowadze pomiędzy produkcją a neutralizacją reaktywnych form tlenu (RFT). Gdy równowaga redox zostaje zachwiana, zaczynają się problemy: stres oksydacyjny prowadzi do uszkodzeń DNA, białek i lipidów, a w konsekwencji – do rozwoju chorób przewlekłych. W ostatnich latach coraz częściej mówi się o tym, że wodór molekularny może pełnić istotną rolę w regulacji tych procesów.
RFT w fizjologii i patologii organizmu to temat złożony, a wodór jako selektywny antyoksydant zyskuje uznanie naukowców (choć wciąż wymaga potwierdzenia w dużych RCT). W oparciu o najnowsze prace – m.in. badania nad wpływem wodoru na szlaki sygnałowe Nrf2 i NF-κB – można powiedzieć jedno: równowaga redox i RFT to system naczyń połączonych, w którym wodór zdaje się pełnić funkcję subtelnego regulatora, a nie brutalnego „czyściciela” rodników. Jeśli chcesz zrozumieć, jak działa, warto też zerknąć na mechanizmy działania terapii wodorem molekularnym.
- czym dokładnie są reaktywne formy tlenu i jakie mają funkcje,
- jak stres oksydacyjny wpływa na patogenezę chorób,
- dlaczego wodór molekularny nie działa jak klasyczny antyoksydant,
- co pokazują najnowsze badania in vitro, in vivo i kliniczne,
- jak terapia wodorem może wspierać naturalne mechanizmy obronne organizmu.
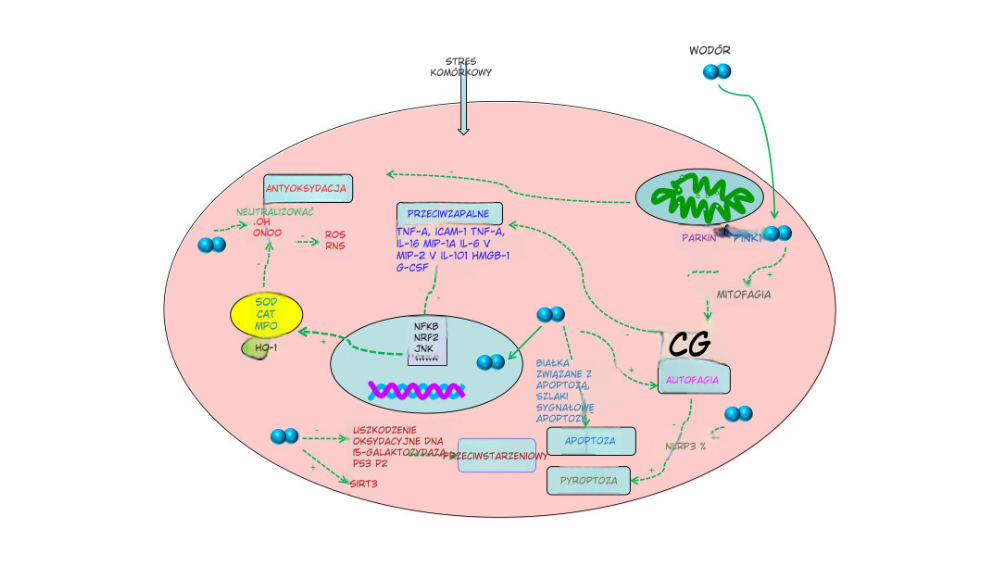
Znaczenie reaktywnych form tlenu w fizjologii człowieka
Reaktywne formy tlenu (RFT) to cząsteczki zawierające tlen w stanie wzbudzonym, zdolne do utleniania innych związków. Wytwarzane są głównie w mitochondriach, gdzie biorą udział w procesie oddychania komórkowego i regulacji sygnalizacji wewnątrzkomórkowej. W fizjologii człowieka pełnią rolę sygnalistów, wpływając na ekspresję genów, proliferację komórek i procesy odpornościowe. Równowaga redox między ich produkcją a neutralizacją przez enzymy antyoksydacyjne, takie jak superoksyd dysmutaza, katalaza i glutation peroksydaza, jest kluczowa dla utrzymania homeostazy.
Nie wszystkie RFT są szkodliwe. Małe ich ilości działają korzystnie, inicjując adaptacyjne odpowiedzi komórkowe (tzw. mitohormezja). Dopiero nadmiar prowadzi do stresu oksydacyjnego i uszkodzeń struktur komórkowych. Mechanizmy obrony oksydacyjnej obejmują zarówno endogenne enzymy, jak i przeciwutleniacze egzogenne – witaminy C, E, karotenoidy czy polifenole. Warto jednak pamiętać, że równowaga oksydacyjno-redukcyjna komórki jest dynamiczna i zależy od tkanki, wieku oraz stanu fizjologicznego.
W licznych opracowaniach porównuje się efektywność neutralizowania najbardziej toksycznych form tlenu, jak rodnik hydroksylowy (•OH). To właśnie on odpowiada za największe uszkodzenia oksydacyjne w komórkach. Zrozumienie jego roli jest punktem wyjścia do tworzenia nowych strategii terapeutycznych i ujęcia problemu całościowo.
| Rodzaj RFT | Źródło | Efekt biologiczny | Enzym neutralizujący | Poziom toksyczności |
|---|---|---|---|---|
| Superoksyd (O₂•⁻) | Łańcuch oddechowy | Sygnalizacja komórkowa | Superoksyd dysmutaza | Umiarkowany |
| Peroksyd wodoru (H₂O₂) | Utlenianie NADPH | Regulacja ekspresji genów | Katalaza | Niski–średni |
| Rodnik hydroksylowy (•OH) | Reakcja Fentona | Uszkodzenie DNA i lipidów | Brak specyficznego enzymu | Bardzo wysoki |
| Tlen singletowy (¹O₂) | Fotoreakcje | Peroksydacja lipidów | Karotenoidy | Wysoki |
| Tlenek azotu (NO•) | Szlak L-argininy | Rozszerzanie naczyń | Hemoglobina | Umiarkowany |
Mechanizmy odpowiedzi oksydacyjnej w patologii organizmu
Wpływ stresu oksydacyjnego na metabolizm komórkowy
W warunkach patologicznych nadmierna produkcja RFT, zwłaszcza w mitochondriach, prowadzi do dysfunkcji energetycznych, peroksydacji lipidów i aktywacji ścieżek zapalnych. Komórki odpornościowe, takie jak neutrofile czy makrofagi, produkują dodatkowe rodniki w ramach reakcji obronnej, co przy braku równowagi redox pogłębia uszkodzenia. W chorobach takich jak cukrzyca, miażdżyca czy neurodegeneracje zaobserwowano wyraźny wzrost markerów stresu oksydacyjnego, w tym malonodialdehydu i 4-hydrononenalu.
Rola inflamasomu i apoptozy komórkowej
Aktywacja inflamasomu NLRP3 przez RFT odgrywa kluczową rolę w regulacji odpowiedzi zapalnej. RFT wpływają na proces apoptozy poprzez uszkadzanie mitochondriów i uwalnianie cytochromu c. Wyniki badań in vivo sugerują, że redukcja poziomu RFT może ograniczać stan zapalny i poprawiać funkcje mitochondriów.
Sygnalizacja przez NF-κB i Nrf2
Dwa kluczowe szlaki sygnałowe – NF-κB i Nrf2 – stanowią przeciwstawne bieguny regulacji oksydacyjno-zapalnej. NF-κB aktywuje ekspresję cytokin prozapalnych, natomiast Nrf2 reguluje ekspresję enzymów antyoksydacyjnych. W badaniach na szczurach z zastosowaniem wody bogatej w wodór wykazano, że modulacja tych ścieżek może znacząco obniżać przewlekły stan zapalny jelit.
W skrócie – nadmiar RFT prowadzi do błędnego koła stresu oksydacyjnego, gdzie uszkodzenia mitochondriów nasilają ich własną produkcję RFT. W tej dynamicznej równowadze nawet tak prosty związek jak nadtlenek wodoru może działać zarówno jako regulator, jak i czynnik szkodliwy – w zależności od kontekstu biologicznego.
Terapia wodorem a równowaga redox w komórkach
Wodór molekularny (H₂) działa selektywnie – reaguje z najbardziej toksycznymi formami tlenu, jednocześnie nie zaburzając fizjologicznej sygnalizacji redoxowej. Badania przeprowadzone na modelach zwierzęcych i komórkowych pokazują, że wodór zmniejsza akumulację lipidów i chroni komórki wątrobowe (HepG2) przed uszkodzeniami oksydacyjnymi poprzez aktywację AMP-kinazy. Woda bogata w wodór przywraca też równowagę redox w modelach z nadmiarem peroksydu wodoru.
Efekty te wydają się wynikać z jego możliwości przenikania przez błony komórkowe i mitochondria – to unikalna cecha, której brakuje większości klasycznych antyoksydantów. W odniesieniu do terapii, wodór nie zastępuje enzymów antyoksydacyjnych, lecz uzupełnia ich działanie. W efekcie wspiera enzymy takie jak superoksyd dysmutaza i katalaza, stabilizując czynność redoxową komórki.
Ciekawych danych dostarcza również analiza wpływu wodoru na peroksydację lipidów i aktywność enzymów redox, zestawiona w badaniu nad wątrobą szczurów. Skuteczność jego działania zależała od poziomu stresu tlenowego i formy podania – wody, inhalacji lub kąpieli gazowych. W podobny sposób reaguje też anionorodnik ponadtlenkowy, którego znaczenie w metabolizmie opisano w kontekście szczegółowej kontroli szlaku mitochondrialnego.
| Rodzaj badania | Model | Efekt działania H₂ | Ścieżka molekularna | Źródło |
|---|---|---|---|---|
| In vivo | Szczury z zapaleniem jelit | Zmniejszenie stanu zapalnego | Nrf2 / NF-κB | MDPI (2022) |
| In vitro | Komórki HepG2 | Redukcja akumulacji lipidów | AMPK | MDPI (2023) |
| In vivo | Myszy narażone na H₂O₂ | Przywrócenie równowagi redox | Antyoksydacyjne enzymy | MDPI (2024) |
| Kliniczne (pilotażowe) | Pacjenci z POChP | Poprawa tolerancji wysiłku | Redukcja stresu oksydacyjnego | PubMed (2022) |
| In vivo | Szczury z nadciśnieniem płucnym | Zmniejszenie zapalenia | Antyoksydacyjne efekty | PubMed (2015) |
Biochemiczne podstawy działania wodoru molekularnego
Interakcje z rodnikami i selektywność reakcji
Wodór reaguje głównie z rodnikiem hydroksylowym i nadtlenoazotynem, co ogranicza toksyczne skutki stresu oksydacyjnego. Reakcje te nie wpływają jednak na pożądane sygnały komórkowe generowane przez umiarkowane stężenia RFT. Badania sugerują, że to właśnie selektywność działania odróżnia H₂ od klasycznych przeciwutleniaczy.
Wpływ na transkrypcję genów i szlaki sygnałowe
Regulacja ekspresji genów przez H₂ obejmuje aktywację Nrf2 i hamowanie NF-κB. W efekcie zwiększa się ekspresja enzymów ochronnych, a spada poziom mediatorów zapalnych. To mechanizm, który w badaniach MDPI pokazano jako kluczowy dla poprawy równowagi redox w modelach zapalenia jelit.
Znaczenie mitochondriów w odpowiedzi na wodór
Mitochondria są głównym miejscem powstawania RFT. Wodór redukuje ich nadmierną aktywność oksydacyjną, przeciwdziałając dysfunkcji i apoptozie. Mechanizm ten tłumaczy częściowo poprawę funkcji metabolicznych obserwowaną w badaniach na zwierzętach i ludziach.
Mechanistyczna precyzja H₂ – zdolność do reagowania tylko z wybranymi RFT, zwłaszcza w mitochondriach – pozostaje jednym z najciekawszych tematów badawczych w terapii wodorem. Więcej o tym, jak wodór reaguje z tymi cząstkami, znajdziesz w opracowaniu dotyczącym jego selektywności reakcji z RFT.
Perspektywy kliniczne i bezpieczeństwo terapii wodorem
Do tej pory większość danych pochodzi z badań in vitro i in vivo, choć pierwsze próby kliniczne są obiecujące. Zaobserwowano możliwy efekt wspomagający przy nadciśnieniu płucnym, astmie czy chorobach metabolicznych. Badania metaanalityczne są nadal nieliczne, ale dostępne wyniki pozwalają stwierdzić, że wodór może pełnić rolę uzupełniającą w strategii redukcji stresu oksydacyjnego.
Pod względem bezpieczeństwa – wodór uznawany jest za nietoksyczny, a jego stosowanie nie wywołuje efektów ubocznych w krótkim okresie. Brakuje jednak danych długoterminowych, dlatego każdy przypadek warto konsultować z lekarzem, zwłaszcza w kontekście chorób przewlekłych.
W praktyce klinicznej coraz częściej stosuje się wodę nasyconą H₂, inhalacje lub kąpiele gazowe. Wybór metody zależy od celu terapeutycznego – i tu przydaje się wiedza z opracowania poświęconego metodom podawania wodoru molekularnego. Dalsze badania RCT są jednak niezbędne, by określić dokładne dawki i czas stosowania terapii.
Dlaczego równowaga redox to klucz do zdrowia
Zrozumienie relacji między RFT a wodorem to krok w stronę nowoczesnej medycyny oksydacyjnej. Nie chodzi o całkowitą eliminację rodników, ale o odzyskanie biologicznego balansu. W skrócie: rodniki są potrzebne, dopóki nie wymykają się spod kontroli. A wodór, będąc cząsteczką najmniejszą z możliwych, może pomóc ten balans utrzymać – selektywnie i bez ingerencji w procesy, które są dla życia niezbędne.
Jeżeli temat terapii wodorem wydaje Ci się wart dalszego zgłębienia, odwiedź stronę poświęconą aktualnym badaniom klinicznym w tym zakresie. To doskonały punkt wyjścia do dalszego poznania sposobów, w jakie ta subtelna cząstka może wspierać fizjologię człowieka.
Źródła
- MDPI: Hydrogen-Rich Water Mitigates LPS-Induced Chronic Intestinal Inflammatory Response in Rats
- MDPI: Hydrogen-Rich Alkaline Water Supplementation Restores Redox Balance
- MDPI: HRW Reduces Lipid Accumulation Through AMPK Activation
- PubMed: Molecular hydrogen as a therapeutic agent for pulmonary disease
- PubMed: Hydrogen ameliorates pulmonary hypertension in rats
- PubMed: Hydrogen-Rich Water Mitigates LPS-Induced Inflammatory Response
FAQ – najczęściej zadawane pytania o RFT i wodór
Czy terapia wodorem może zastąpić standardowe leczenie?
Nie. Wodór molekularny może pełnić rolę wspomagającą, ale nie zastępuje leczenia farmakologicznego. Może uzupełniać terapię, zmniejszając stres oksydacyjny, jednak decyzje terapeutyczne muszą być podejmowane przez lekarza prowadzącego.
Jak długo trzeba stosować wodór, aby odczuć efekty?
Badania kliniczne sugerują, że efekty subiektywne, takie jak poprawa samopoczucia czy zmniejszenie zmęczenia, mogą wystąpić po kilku tygodniach regularnego stosowania. Długotrwałe efekty wymagają dalszych badań i zależą od schorzenia.
Czy wodór można łączyć z klasycznymi przeciwutleniaczami?
Tak, ale z umiarem. Wodór działa inaczej niż witaminy antyoksydacyjne – nie „czyści” wszystkich RFT, a jedynie te najbardziej reaktywne. Dzięki temu ryzyko nadmiernego zahamowania procesów redox jest niewielkie.
Czy wodór wpływa na proces starzenia się?
Zaobserwowano możliwy efekt spowolnienia procesów starzenia poprzez redukcję stresu oksydacyjnego w mitochondriach i poprawę ekspresji enzymów naprawczych DNA. To obiecujący, choć wciąż badany kierunek w gerontologii molekularnej.
Jakie formy podawania wodoru są najskuteczniejsze?
Najczęściej stosuje się inhalacje mieszanką H₂/O₂ oraz picie wody nasyconej wodorem. Wybór zależy od celu – inhalacje szybciej wpływają na układ oddechowy, natomiast woda działa bardziej ogólnoustrojowo.
Czy terapia wodorem ma przeciwwskazania?
Na ten moment nie stwierdzono istotnych przeciwwskazań, ale ostrożność zachowuje się u osób z ciężkimi chorobami układu oddechowego i sercowo-naczyniowego. Konieczna jest konsultacja z lekarzem.
Jakie są kierunki przyszłych badań nad wodorem?
Nowe projekty skupiają się na wykorzystaniu wodoru w chorobach neurodegeneracyjnych, metabolicznych i autoimmunologicznych. Coraz częściej bada się też jego potencjał w modulacji ekspresji genów i komunikacji międzykomórkowej.

