Wodór molekularny w ostatnich latach zyskał uwagę jako cząsteczka o wyjątkowej zdolności do selektywnego reagowania z reaktywnymi formami tlenu, w tym najbardziej toksycznym hydroksylowym rodnikiem. To nie jest kolejna moda czy próba uproszczenia złożonej biochemii — to twarda fizykochemia i coraz mocniej potwierdzane dane eksperymentalne, zarówno in vitro, jak i w badaniach klinicznych. Co jednak dokładnie sprawia, że H₂ działa inaczej niż inne przeciwutleniacze? Dlaczego jest tak selektywny? O tym właśnie będzie ten tekst.
W dużym skrócie – wodór molekularny wchodzi w reakcje z najbardziej reaktywnymi formami tlenu (Reactive Oxygen Species, ROS), neutralizując je, a jednocześnie nie zaburza fizjologicznej równowagi redox niezbędnej do sygnalizacji komórkowej. Dzięki temu może wspierać funkcje mitochondrialne, ograniczać peroksydację lipidów i stabilizować równowagę oksydacyjną w komórkach. Więcej o mechanizmach działania można przeczytać na stronie opisującej mechanizmy działania terapii wodorem.
- Jak wodór reaguje z reaktywnymi formami tlenu?
- Jakie procesy molekularne decydują o jego selektywności?
- Jakie korzyści obserwuje się w badaniach terapeutycznych?
- Jakie są potencjalne ograniczenia i ryzyka?
- Jak wygląda przyszłość terapii wodorem w medycynie?
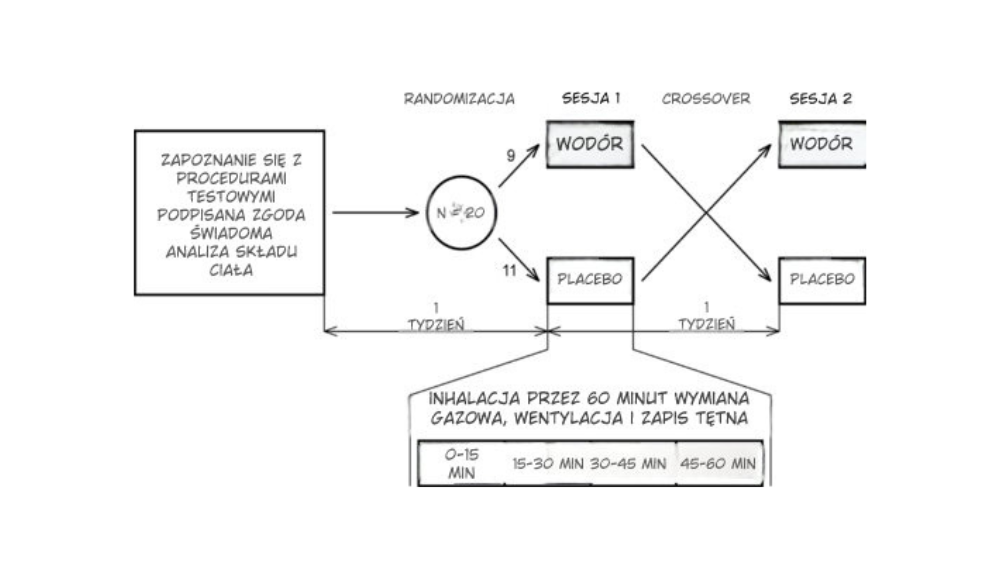
Mechanizm reakcji wodoru molekularnego z reaktywnymi formami tlenu
Reaktywne formy tlenu (RFT), takie jak hydroksylowy rodnik (•OH) czy anionorodnik ponadtlenkowy (O₂•−), powstają naturalnie w procesach metabolicznych. Ich nadmiar prowadzi do stresu oksydacyjnego, który uszkadza błony komórkowe, DNA i białka. Wodór molekularny (H₂) działa inaczej niż klasyczne antyoksydanty – nie wiąże się ze wszystkimi rodnikami, lecz wybiórczo reaguje z najbardziej reaktywnymi i toksycznymi z nich, pozostawiając inne cząstki sygnałowe, kluczowe dla funkcjonowania komórek.
Badania modelowe opisane w artykule Molecular Hydrogen as an Antioxidant and Radioprotector wskazują, że H₂ redukuje rodniki hydroksylowe poprzez reakcje kaskadowe oparte na mikrośrodowisku wodnym i z udziałem enzymów antyoksydacyjnych. W symulacjach Monte Carlo wykazano, że H₂ może ograniczać efekt wtórnej generacji ROS w mitochondriach, co ma istotne znaczenie przy hamowaniu toksyczności oksydacyjnej.
W tabeli poniżej przedstawiono główne rodniki i ich potencjalne reakcje z wodorem molekularnym:
| Rodnik / RFT | Źródło | Reaktywność | Efekt interakcji z H₂ | Pewność dowodowa |
|---|---|---|---|---|
| Hydroksylowy rodnik (•OH) | Promieniowanie jonizujące | Bardzo wysoka | Neutralizacja do H₂O | Potwierdzone in vitro |
| Superoksyd anionowy (O₂•−) | Mitochondrialne łańcuchy oddechowe | Średnia | Brak bezpośredniej reakcji | Wysoka |
| Nadtlenek wodoru (H₂O₂) | Utlenianie białek i lipidów | Umiarkowana | Brak reakcji bez katalizatora | Średnia |
| Tlen singletowy (¹O₂) | Fotosensybilizacja | Wysoka | Pośrednie ograniczenie generacji | Średnia |
| Rodnik peroksylowy (ROO•) | Łańcuchy lipidowe | Wysoka | Redukcja pośrednia | Niska |
Omawiając genezę stresu oksydacyjnego, warto spojrzeć na szerszy kontekst równowagi redox, o czym przeczytasz w materiale poświęconym stresowi oksydacyjnemu i jego skutkom.
Rola wodoru w regulacji równowagi redox i ekspresji genów antyoksydacyjnych
Wodór molekularny nie tylko eliminuje nadmiar reaktywnych form tlenu, ale także wpływa na równowagę redox poprzez modulację ekspresji genów związanych z szlakiem sygnałowym Nrf2. Ten szlak odpowiada za aktywację enzymów takich jak peroksydaza glutationowa (GPx) i dysmutaza ponadtlenkowa (SOD), które stanowią naturalną linię obrony przeciwko stresowi oksydacyjnemu.
Aktywacja szlaku Nrf2
Szlak Nrf2 odpowiada za utrzymanie homeostazy mitochondrialnej oraz regulację ekspresji genów kodujących enzymy antyoksydacyjne. W badaniach in vivo wykazano, że H₂ zwiększa aktywność Nrf2, co prowadzi do stabilizacji procesów redox w obrębie mitochondriów i ograniczenia apoptozy komórkowej.
Modulacja szlaku NF-κB
Wodór może również hamować aktywność szlaku NF-κB, związanego z reakcjami zapalnymi. To tłumaczy jego działanie przeciwzapalne i cytoprotekcyjne w przypadkach przewlekłego stresu oksydacyjnego i zapalenia tkanek.
Indukcja endogennych przeciwutleniaczy
Zauważono też, że ekspozycja organizmu na H₂ może zwiększyć aktywność endogennych przeciwutleniaczy, takich jak glutation, katalaza i tioredoxyna. Ta adaptacyjna reakcja wskazuje na potencjalną zdolność wodoru do przywracania równowagi nawet w warunkach przewlekłego stresu oksydacyjnego.
Pełny przegląd biologicznych definicji stresu oksydacyjnego znajdziesz na stronie opisującej stres oksydacyjny w biologii komórki.
Efekty kliniczne terapii wodorem molekularnym
Badania kliniczne nad terapią wodorem molekularnym obejmują różne drogi podawania: inhalację, spożywanie wody nasyconej H₂ oraz aplikacje transdermalne. W badaniu pilotażowym Topically Applied Molecular Hydrogen Normalizes Skin Parameters zaobserwowano poprawę parametrów skóry związanych z markerami stresu oksydacyjnego, co sugeruje działanie antyoksydacyjne i przeciwzapalne.
Inne badania, jak Molecular hydrogen: An inert gas turns clinically effective, opisują pozytywne skutki terapii u pacjentów z przewlekłymi chorobami metabolicznymi i neurodegeneracyjnymi. Efekty obejmowały redukcję markerów zapalnych, poprawę funkcji mitochondrialnych oraz zwiększenie saturacji tlenem (potwierdzone także w badaniu dotyczącym chorób płuc).
| Zastosowanie | Rodzaj badań | Efekt | Mechanizm | Status dowodów |
|---|---|---|---|---|
| Astma i POChP | In vivo, kliniczne | Redukcja cytokin prozapalnych | NF-κB | Średni |
| Choroby neurodegeneracyjne | Kliniczne, obserwacyjne | Poprawa funkcji poznawczych | Ochrona mitochondriów | Niski |
| Radioprotekcja | In vitro, model komórkowy | Ograniczenie uszkodzeń DNA | Zwi. z redukcją ROS | Wysoki |
| Stres metaboliczny | RCT na zdrowych | Modulacja metabolizmu tlenowego | Aktywacja szlaku Nrf2 | Średni |
| Urazy skóry | Pilotowe | Szybsza regeneracja | Zwiększona aktywność GPx | Niski |
W kontekście środowiskowych źródeł stresu oksydacyjnego warto zajrzeć na opracowanie dotyczące źródeł stresu oksydacyjnego.
Potencjalne zastosowania i ograniczenia terapii wodorem molekularnym
Terapia wspomagająca w chorobach przewlekłych
Wodór może pełnić rolę wsparcia w leczeniu chorób przewlekłych, takich jak cukrzyca, nadciśnienie czy choroby neurodegeneracyjne. Jego działanie neuroprotekcyjne i mitochondrialna stabilizacja mogą sprzyjać utrzymaniu zdrowia komórkowego. Jednak badania są nadal ograniczone i wymagają standaryzacji sposobu podawania.
Bezpieczeństwo i skutki uboczne
Dotychczasowe dane wskazują, że wodór jest dobrze tolerowany, a ryzyko działań niepożądanych minimalne. Należy jednak podkreślić brak długoterminowych danych dotyczących stosowania u osób z chorobami przewlekłymi.
Standaryzacja stężeń i metod podawania
Skuteczność terapii zależy od drogi dostarczenia wodoru do tkanek. Badania z 2024 roku wskazują, że inhalacja H₂ zapewnia szybszy i bardziej stabilny efekt redox niż spożywanie wody wzbogaconej wodorem – jednak wymaga to dalszej walidacji w badaniach RCT.
Więcej o konsekwencjach przewlekłego stresu oksydacyjnego znajdziesz na stronie omawiającej skutki stresu oksydacyjnego.
Znaczenie wodoru molekularnego dla zdrowia komórkowego i terapii wspomagających
Obserwacja reakcji wodoru na poziomie molekularnym otwiera nowe kierunki w medycynie regeneracyjnej, terapii przeciwutleniającej i prewencji chorób związanych ze starzeniem. Jego mały rozmiar umożliwia szybki transport przez błony komórkowe, co czyni go unikalnym związkiem bioaktywnym o możliwym zastosowaniu klinicznym.
Stymulacja regeneracji komórek, modulacja odpowiedzi immunologicznej i redukcja uszkodzeń DNA to tylko niektóre z zauważanych efektów. W skrócie — wodór może pełnić rolę „pierwszego strażnika” równowagi redox, ale… potrzebna jest nadal duża ostrożność w interpretacji wyników. Wymagane są dalsze badania RCT i metaanalizy.
Firmy mogą już dziś zapoznać się z zakresem zastosowań opisanych na stronie praktycznych zastosowań terapii wodorem molekularnym.
Dlaczego warto śledzić rozwój terapii wodorem molekularnym
Terapia wodorem molekularnym rozwija się dynamicznie. Coraz więcej ośrodków badawczych potwierdza wpływ H₂ na stres oksydacyjny, funkcję mitochondrialną i procesy starzenia. Dla osób zainteresowanych częścią badawczą lub wdrożeniową – warto zaglądać na stronę Polskiego Instytutu Terapii Wodorem Molekularnym, gdzie sukcesywnie publikowane są analizy najnowszych prac.
Wodór nie jest panaceum, ale w rękach naukowców i lekarzy może stać się ważnym elementem terapii wspomagających w chorobach przewlekłych. W praktyce – to narzędzie, które wymaga precyzji, wiedzy i świadomości biologicznej natury równowagi redox.
Źródła
- Molecular Hydrogen as an Antioxidant and Radioprotector
- Topically Applied Molecular Hydrogen Normalizes Skin Parameters
- Hydrogen Water in Chronic Lung Disease
- Molecular hydrogen: An inert gas turns clinically effective
- Molecular hydrogen inhalation modulates resting metabolism
- Molecular Hydrogen in the Treatment of Respiratory Diseases
FAQ: Najczęściej zadawane pytania o wodór molekularny
Czy wodór molekularny działa natychmiast po podaniu?
Nie zawsze. Efekt przeciwutleniający może pojawić się po kilku minutach, jednak biologiczne skutki – jak regulacja ekspresji genów czy poprawa funkcji mitochondrialnej – wymagają regularnego stosowania przez dni lub tygodnie.
Czy inhalacja wodoru jest bezpieczna dla osób starszych?
Dotychczasowe dane nie wskazują na przeciwwskazania, jednak u seniorów z niewydolnością oddechową zalecana jest kontrola lekarska, gdyż zmieniająca się pojemność płuc wpływa na dystrybucję gazu.
Jak rozpoznać dobre urządzenie do terapii wodorem?
Warto zwracać uwagę na certyfikaty CE lub ISO oraz wyniki pomiaru stężenia H₂ wytwarzanego przez urządzenie. Na stronie instytutu dostępne są szczegóły dotyczące certyfikacji urządzeń.
Czy wodór może wpływać na układ odpornościowy?
Tak, badania wskazują, że H₂ może modulować profil cytokinowy i obniżać stężenie markerów zapalnych. Jest to jednak działanie pośrednie, wynikające z obniżenia stresu oksydacyjnego.
Czy wodór reaguje z antyoksydantami w diecie?
Nie bezpośrednio. H₂ działa na poziomie reaktywnych form tlenu, podczas gdy klasyczne antyoksydanty (np. witamina C) uczestniczą w niezależnych reakcjach redox. Połączenie ich efektów może być synergiczne.
Jak długo utrzymuje się efekt po inhalacji wodoru?
Efekt biochemiczny utrzymuje się od kilkunastu minut do kilku godzin, w zależności od stężenia i czasu ekspozycji. Przy regularnym stosowaniu może dochodzić do adaptacji metabolicznej organizmu.
Czy wodór może wspierać regenerację po wysiłku fizycznym?
Tak, wykazano, że H₂ może zmniejszać peroksydację lipidów i uszkodzenia mięśniowe po treningu. Wynika to ze zdolności do neutralizacji rodników powstających w mitochondriach podczas intensywnego metabolizmu tlenowego.

